| Typ |
Ketten |
Aufbau der Dreifachhelix |
Dreifachhelix Länge, Strukturdetails |
Vorkommen, Besonderheiten |
| Kollagene, die lange Fibrillen mit 67
nm-Periodizität ausbilden, die aus mehreren Kollagentypen zusammengesetzt
sein können (z.B. II + XI oder I + III + V) |
|
I
|
a1(I); a2(I) |
[a1(I)]2[a2(I)] |
300 nm; Fibrillendurchmesser 50 bis maximal 200 nm
Ketten 1.050 Aminosäuren lang; |
Unterhautbindegewebe, Sehne,
Knochen,
Dentin,
Sklera & Cornea
des Auges, in so gut wie allen Bindegewebsarten
außer Knorpel |
|
If
|
a1(I); a2(I) |
[a1(I)]3 |
300 nm |
fetale Form |
|
II
|
a1(II) |
[a1(II)]3 |
300 nm; Durchmesser nur ca. 30 nm;
von visköser Proteoglykanmatrix überzogen |
hyaliner- und Faserknorpel,
Glaskörper des Auges,
Chorda dorsalis, Tectorialmembran
des Innenohrs |
|
III
|
a1(III) |
[a1(III)]3 |
300 nm; Durchmesser ca. 40 nm; meist mit Typ I |
in Typ I Fibrillen, bilden retikuläre
Fasern, lockeres Bindegewebe,
Unterhautbindegewebe, Muskel,
Blutgefäßwände |
|
V
|
a1(V); a2(V);
a3(V) |
[a1(V)]3, [a1(V)]2[a2(V)]
und [a1(V)][a2(V)][a3(V)] |
390 nm; N-terminale globuläre Domäne;
meist zusammen mit Typ I |
in Typ I Fibrillen, fetale Gewebe + Membranen; interstitielles Gewebe,
Tectorialmembran, um glatte
Muskelzellen, Corium, Knochen,
Plazenta |
|
XI
|
a1(XI); a2(XI);
a3(XI) |
[a1(XI)][a2(XI)][a3(XI)] |
300 nm; oft mit Typ II, dünne Fasern |
in Typ II Fibrillen, hyaliner Knorpel,
Tectorialmembran |
| Fibrillen-assoziierte Kollagene einer Dreifachhelix, die
durch globuläre Domänen unterbrochen wird |
|
IX
|
a1(IX); a2(IX);
a3(IX) |
[a1(IX)][a2(IX)][a3(IX)] |
200 nm; N-terminale globuläre Domäne;
kovalent oberflächlich an Typ II gebunden |
hyaliner Knorpel, Glaskörper, Tectorialmembran,
bindet Glykosaminoglykane |
|
XII
|
a1(XII) |
[a1(XII)]3 |
große N-terminale globuläre Domäne; kreuzförmiges
Molekül; außen an Kollagen Typ I gebunden |
embryonale Sehnen, Unterhautbindegewebe,
Hornhaut (Cornea) des Auges |
|
XIV
|
a1(XIV) |
[a1(XIV)]3 |
große N-terminale globuläre Domäne;
kreuzförmiges Molekül |
fetales Unterhautbindegewebe,
Sehnen |
| Fibrillen-assoziierte Kollagene, die perlschnurartige Filamente
bilden |
|
VI
|
a1(VI); a2(VI);
a3(VI) |
[a1(VI)][a2(VI)][a3(VI)] |
150 nm; N- und C-terminale globuläre Domäne;
Banden mit 150 nm Periodik; Typ I assoziiert |
in den meisten interstitiellen Geweben, am Übergang von Muskeln
zu Sehnen,
perizelluläre Knorpelmatrix,
in den Wänden von Blutgefäßen,
im Endomysium |
| Kollagene, die sich blattförmig anordnen |
|
IV
|
a1 bis 5(IV) |
[a1(IV)]2[a2(V)]
und andere Formen |
60 nm lange Dreifachhelixregion und 40 nm lange
globuläre Domänen; Bildung von Tetrameren |
alle Basalmembranen, Ausbildung eines
zweidimensional verknüpften Netzwerks,
wird gebildet von Endothel- und Epithelzellen,
Gliazellen
und Fettzellen |
|
VIII
|
a1(VIII); a2(VIII) |
? |
reguläres dreieckiges Gitter |
subendotheliales Gewebe, Descement-Membran
der Hornhaut am Auge |
|
X
|
a1(X) |
[a1(X)]3 |
150 nm; C-terminale globuläre Domäne |
wird von hypertrophen Knorpelzellen
gebildet, daher in der
Epiphysenfuge bei der Knochenmineralisation |
| Kollagene, die Ankerfibrillen bilden |
|
VII
|
a1(VII) |
[a1(VII)]3 |
450 nm; Dimer; an beiden Enden globuläre Domäne |
bildet die kurzen Ankerfibrillen, die die Basallamina
von Epithelien mit dem darunter-
liegenden lockeren Bindegewebe
verbinden im Fall eine Basalmembran gebildet
wird |
| Kollagene, für die bisher nur die c-DNA nachgewiesen
wurde |
|
XIII
|
a1(XIII) |
? |
? |
nur C-DNA dafür in Endothelzellen
gefunden |
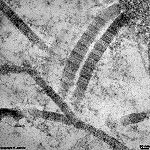
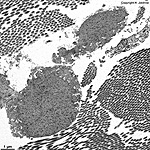
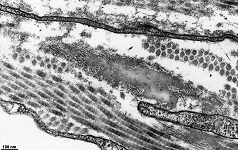
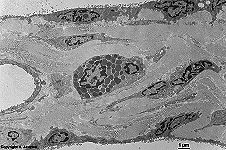
Die häufigsten Typen sind I, II und III. Im elektronenmikroskopischen
Längsschnitt zeigen die Typen I, II, III, V, XI eine typische